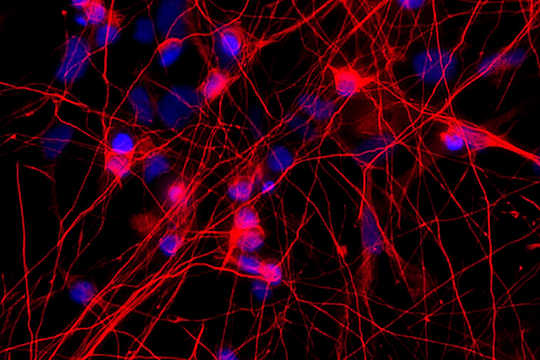
Fotoğrafta MAPT genindeki mutasyonlu nöronlar (kırmızı) gösteriliyor - proteini tau yapan bir gen. Bu mutasyonu olan insanlar frontotemporal demans geliştirir. (Kredi: Sidhartha Mahali)
Bilim adamları, kalıtımsal bir frontotemporal demans formuna neden olan tek bir gende yalnız bir mutasyon keşfettiler, beyindeki nöronların birbirleriyle iletişim kurmasını zorlaştırarak nörodejenerasyona neden oluyorlar.
Sık görülen Alzheimer hastalığının aksine, frontotemporal demans gençleri etkileme eğilimindedir. Hastalığı olan insanlar genellikle erken 60'lerinde hafıza kaybına uğrarlar, ancak bazı insanları 40'leri kadar genç etkileyebilir. Erken başlangıçlı bunama vakalarının% 20'ini oluşturan bu durum için etkili bir tedavi yoktur.
Yeni bulgular, Alzheimer hastalığında bilişsel gerileme ile ilişkili olarak tau adı verilen bir protein yapan MAPT geninde sıfırdır. Mutasyonun aşağı yönde etkilerini belirlemek, frontotemporal demans, Alzheimer hastalığı ve Parkinson hastalığı dahil olmak üzere tau ile ilişkili diğer hastalıklar için yeni tedavi hedeflerinin belirlenmesine yardımcı olabilir.
St. Louis'deki Washington Üniversitesi psikiyatri profesörü Celeste M. Karch, “Bireyin beyninde de görünen bir tabakta kültürlenmiş insan hücrelerinde frontotemporal demansla birlikte görülen değişiklikleri yakalayabileceğimizi gösterdik” diyor. Ortaya çıkan makalenin kıdemli yazarı Translasyonel Psikiyatri.
“Daha da önemlisi, kullandığımız yaklaşım, hücrelerde ve hasta beyinlerinde FDA tarafından onaylanmış bileşiklerden etkilenmiş olabilecek genlere ve yollara odaklanmamızı sağlıyor. Bu bileşiklerden herhangi birinin frontotemporal demansı olan kişilerde, bozulmuş bu yolların işlevini iyileştirerek hafıza kaybını önleyip önleyemeyeceğini veya hatta hafızayı yeniden sağlayıp sağlayamayacağını değerlendirmek istiyoruz ”diyor Karch.
İletişim arızası
Çalışma için araştırmacılar, MAPT geninde spesifik bir mutasyon olan frontotemporal demans hastalarından deri örnekleri topladı.
Araştırmacılar daha sonra hastaların cilt hücrelerini, vücuttaki herhangi bir hücre tipinde büyüme ve gelişme yeteneğine sahip olan uyarılmış pluripotent kök hücrelere dönüştürdüler. Araştırmacılar, bu kök hücrelere, MAPT mutasyonuna sahip olan nöronlara dönüşerek büyümeleri için onları eşlik eden bileşiklerle tedavi ettiler. Daha sonra, CRISPR adlı gen düzenleme teknolojisini kullanan araştırmacılar, bazı nöronlardaki mutasyonları ortadan kaldırdı, ancak diğerlerinde değil ve olanları gözlemledi.
Psikiyatri profesörü yardımcı kıdemli yazar Carlos Cruchaga, “Mutasyonun nöronların iletişim kabiliyetini değiştirdiğini öne sürerek hücresel iletişim ile ilgili genlerde ve yolaklarda farklılıklar bulduk” diyor.
“MAPT'deki ilk mutasyon, hastalığı başlatan anahtar değişikliktir ve tedavi için potansiyel bir hedeftir, ancak MAPT geninden aşağı akışta, hastalığı tedavi etmek için kullanılabilecek iyi hedefler olan başka genler de var.”
Hasar önleme
Mutasyona sahip nöronlarda, araştırmacılar, beyin nöronları üzerinde GABA reseptörleri yapan genler de dahil olmak üzere 61 genlerinde değişiklikler buldu. GABA reseptörleri, beyindeki ana inhibitör reseptörlerdir ve bunlar, beyin hücreleri arasında birkaç iletişim türü için anahtardır.
Araştırmacılar, hayvan modellerinde deney yaptıklarında GABA reseptörlerini yapan genlerde benzer aksaklıklar tespit etmiş ve frontotemporal demans ile ölen hastalardan gelen beyin dokusunu analiz etmişlerdir. Ayrıca, frontotemporal demansı olan 2,000 hastaları ve düzensiz 4,000 hastaları genomewid bir birliktelik çalışmasından elde ettikleri bulgulara da baktılar. Bu analiz, GABA ile ilişkili genlerin potansiyel hedefler olduğuna da işaret etti.
Harari, “Kök hücre kaynaklı nöronlarımızı kullanarak, insan dokusunda, incelediğimiz postmortem dokularda gördüğümüz nörodejenerasyondan önce bu GABA genlerinin bazılarını hedef alma fırsatına sahibiz” diyor. “En azından hücre kültürlerinde, potansiyel tedavilerin kalıtsal frontotemporal demans biçimlerinin neden olduğu hasarı önleyip önlemediğini öğrenebiliriz.”
Araştırmacılar, nadir görülen kalıtsal beyin hastalıkları formlarını inceleyerek, bu hastalıkların daha yaygın biçimlerinin nasıl tedavi edileceği hakkında çok şey öğreneceklerine inanıyor.
Cruchaga, “Frontotemporal demans ve Alzheimer hastalığının genetik formları, nadir görülen mutasyonlardan kaynaklanmaktadır” diyor. “Fakat bu hastalıkların daha tipik vakalarıyla çok ortak yönleri var. Kalıtsal mutasyonların neden olduğu bu vakaları anlarsak, bu hastalıkların ortak formlarını daha iyi anlamamız gerekir. ”
Ulusal Sağlık Enstitüleri Ulusal Yaşlanma Enstitüsü ve Baskın Olarak Devralınan Alzheimer Ağı, çalışmayı finanse etti. Tau Konsorsiyumu, Alzheimer Derneği, Alman Nörodejeneratif Hastalıklar Merkezi, Raul Carrea Nörolojik Araştırma Enstitüsü, Japonya Tıbbi Araştırma ve Geliştirme Ajansı, AMED ve Kore Sağlık Endüstrisi Geliştirme Enstitüsü aracılığıyla Kore Sağlık Teknolojisi Ar-Ge projesi ek finansman sağladı .
Kaynak: St. Louis'de Washington Üniversitesi
İlgili Kitaplar
at InnerSelf Pazarı ve Amazon





























